撰文:挑食的免疫喵
来源:闲谈 Immunology
● ● ●
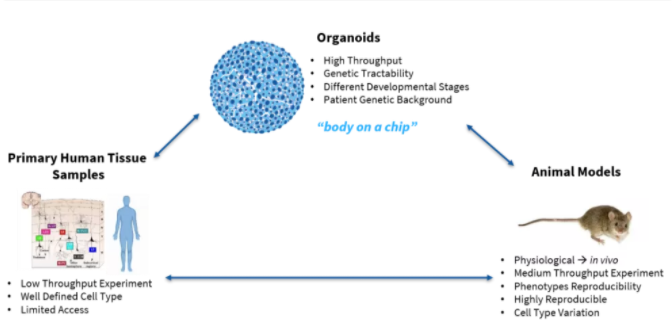
提起类器官,大家的第一反应也许是这样的:在培养皿中,一个小小的器官悄然生长着……类器官(Organoid)是在体外用3D培养技术对干/祖细胞进行诱导分化形成的在结构和功能上都类似目标器官/组织的三维细胞复合体。类器官其具有稳定的表型和遗传学特征,能够在体外长期培养。
类器官是2017年度Nature Methods评选的方法, 细胞可来源于人体,结构类似于器官,则可以作为接近人体的研究模型, 进行科学研究和药物筛选。
1
类器官的培养
成体干细胞衍生的类器官培养,通常是将制备好的成体干细胞单细胞悬液,加入到细胞外基质(ECM)水凝胶中来建立的。比如肠道类器官,从小肠或结肠分离出的隐窝细胞可以培养出类器官,从分离的成人肠干细胞中也可以培养出类器官。
上皮类器官的培养基,是以添加与其器官相关的生长因子培养基为基础的。因此,从不同组织(如呼吸道、肝脏、胰腺、皮肤、膀胱、大脑、心脏)提取的细胞,要在培养基中补充相关生长因子。
大脑类器官培养过程如下图:
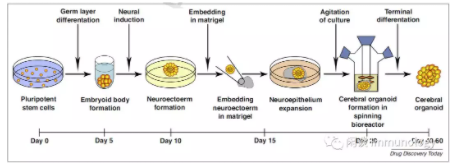
大脑类器官培养过程
诱导多能干细胞(iPSC)衍生细胞,在神经诱导介质中生长,产生神经外胚层,嵌入凝胶中,并在旋转生物反应器或轨道摇床中生长,以更好地扩散,获得3D类脑器官。在暴露于维甲酸的情况下,大脑器官通过自我组装模式,形成自缔和组织,形成包括放射状胶质细胞在内的不同种群的神经祖细胞,这些神经祖细胞扩展形成大脑结构。
2
上皮细胞类器官的构建
一般来说,上皮细胞出现在机体和外界先接触的器官(比如皮肤,气管,肺,消化道),是机体对抗病原体侵染的第一层屏障,也是第一个对病原体感染作出反应的细胞。
为了维持体内平衡,并提供对感染的快速反应,上皮细胞与免疫细胞密切配合。所以在上皮区域,也是全身免疫细胞浓度最高的区域。建立上皮细胞和免疫细胞相互作用的模型,是研究抗感染免疫和损伤后免疫的重要手段。
上皮细胞类器官的建立,可以非常精准的模拟机体上皮环境,也被发展起来研究上皮和免疫细胞相互作用。
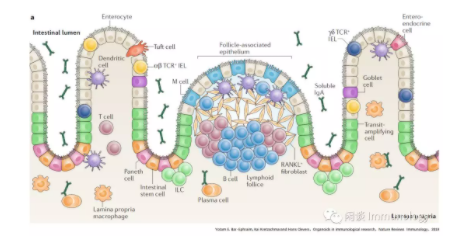
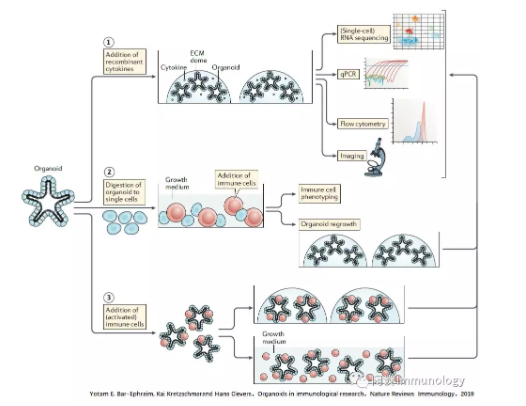
有三种共培养的模式
用细胞外基质中的重组细胞因子处理类器官,用以评价免疫细胞衍生细胞因子对于上皮细胞的影响。(如IL-4和IL-13促进丛生细胞分化,而IL-22支持干细胞增殖和存活。)
将器官消化到单个细胞,在免疫细胞存在的情况下培养生长。用以评估免疫细胞和免疫细胞衍生的细胞因子(可溶性或膜结合)对器官生长和分化的影响,以及上皮细胞对免疫细胞表型的影响。
在ECM或生长培养基(悬浮培养)中,向完整的类器官中添加免疫细胞(如 T 细胞或ILCs),用以评估免疫细胞与上皮细胞之间的相互作用。
这些检测的读数通常包含消化形成的器官和随后的转录(无论是单细胞RNA测序或定量PCR),成像和/或流式细胞术评估上皮细胞和/或免疫细胞表型。
在这些共培养中使用的免疫细胞,要么直接从小鼠组织(例如,脾细胞、肠上皮内淋巴细胞、T细胞、ILCs或肺ILC2s)中分离。要么直接从人外周血中提取,要么先在体外分化。
3
胸腺类器官:用于研究 T 细胞发育
胸腺是 T 细胞从祖细胞向成熟幼稚淋巴细胞分化的中心部位。来自骨髓的 T 淋巴祖细胞,在胸腺皮质进行阳性选择,随后在胸腺髓质中进行阴性选择。胸腺由两种上皮细胞组成:皮质胸腺上皮细胞(cTECs)和髓质胸腺上皮细胞(mTECs)。
3D重建胸腺类器官被证明是模拟其功能的关键。几种胸腺类器官的产生方法:1)胸腺类器官培养通常是来自人细胞系或胎鼠或新生小鼠胸腺组织。2)TEC样细胞与人胚胎干细胞的体外分化。
这些培养都产生胸腺样结构。在体外产生活的 T 淋巴细胞,并在移植到裸鼠上时发挥作用。有趣的是,虽然类似胸腺结构的长时间培养是可能的(离体培养长达56天),但在连续传代时,细胞失去了集落形成能力。重要的是,虽然在成年小鼠中已经发现了一种双能的TEC前体,但含cTECs和mTECs的胸腺器官尚未从单个干细胞中生成。此外,考虑到小鼠体内某些双能TEC前体的生长因子已被发现(如BMP-4和IL-2),可以尝试这些因子是否可用于维持TEC的祖细胞来源的类器官。
4
类器官模型:用于病原体感染研究
幽门螺杆菌微量注射到人源iPSC来源的胃类器官,在那里它与上皮紧密相连,并随后转移毒力因子细胞毒素相关基因A(CAGA)进入上皮细胞。幽门螺杆菌诱导iPSC衍生的胃器官中表达检查点PDL1,可能导致免疫逃逸。实际上,在没有PD1阻断抗体的情况下,自体细胞毒性T淋巴细胞(CTLs)对类器官没有任何作用。因而类器官不但可以模拟感染的病理过程,也可以作为模型进行药物作用机理研究。
类器官模型也被用于艰难梭菌感染肠道上皮细胞,呼吸道合胞病毒感染肺上皮细胞等的研究。
5
类器官模型:用于组织修复和再生
免疫系统也会参与上皮损伤后的组织修复。例如,ILC3细胞分泌的IL-22保护肠道免受辐射、化疗或 GVHD 的损害。如上所述,IL-22独立于其他因素和Paneth细胞的存在,诱导LGR5-ISCs的存活和增殖。
促炎细胞因子TNF,通过NF-κB依赖的方式促进原代小鼠肝细胞类器官的长期培养,而非IL-6。然而重要的是,小鼠和人的类器官都可以在没有TNF的情况下生长,这表明虽然低度炎症是上皮再生所必需的,但在稳态条件下不需要。类器官为组织损伤修复及再生提供了类似于机体环境的模型。
6
类器官模型:用于肿瘤微环境研究
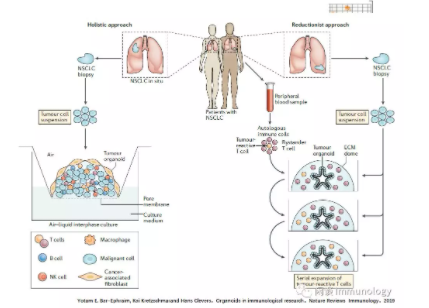
两种主要的方式被使用(以非小细胞肺癌为例)
在整体方法(左)中,肿瘤活检组织是在气液界面间环境培养。所有肿瘤细胞类型(包括内源性免疫细胞和其他非上皮细胞类型)的细胞悬液,皆可促进肿瘤特异性T细胞的生长。
在还原模拟法(右)中,上皮类器官是从肿瘤活检组织中生长出来的,然后与来自同一患者外周血的自体免疫细胞共培养,以促进肿瘤反应细胞的连续扩张。
虽然整体方法,允许包括整个肿瘤微环境的肿瘤材料的培养。因此,与体内情况非常相似,但不易长时间维持,而还原模拟方法允许肿瘤上皮的长期培养和扩展,这使得广泛长期的研究成为可能。
7
类器官:用于药物筛选
一)心肌类器官
动物模型(主要是小鼠),被广泛用于研究心脏病,提供有价值的结果。然而,由于许多功能和生物学特性的物种差异很大,它们对人类心脏疾病和药物安全性的推断很差。
人类多能干细胞(包括ESC和iPSC)可以提供无限的人类心肌细胞,有可能弥合这一鸿沟。然而,传统 2D 培养中的多能干细胞源性心肌细胞功能缺乏成熟,影响准确预测人类生物学和病理生理学的能力。3D人体类器官提供了更接近的模型,是解决问题的潜在方法。
澳大利亚昆士兰大学的科学家在 Cell Stem Cell 发表文章,他们基于96孔板,培养心脏心肌类器官,进而进行化合物筛选的新流程。
具体流程如下图:
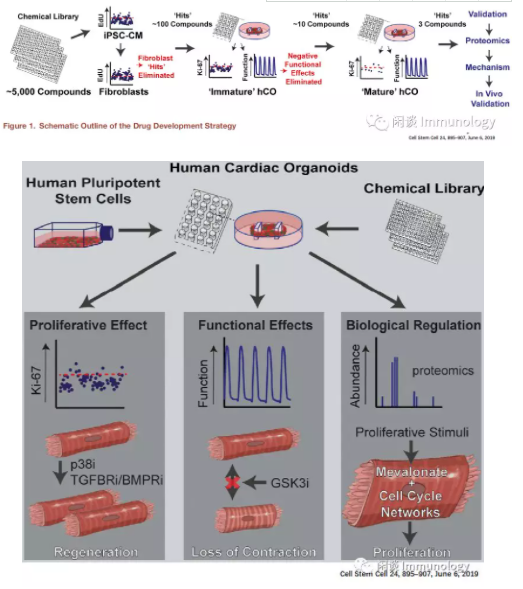
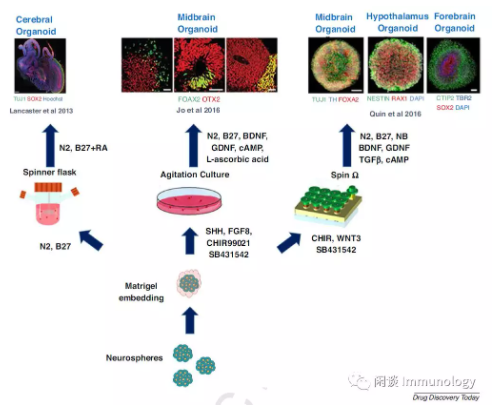
二)大脑类器官
神经球经培养,会产生大脑,中脑,海马,前脑等不同脑部类器官。
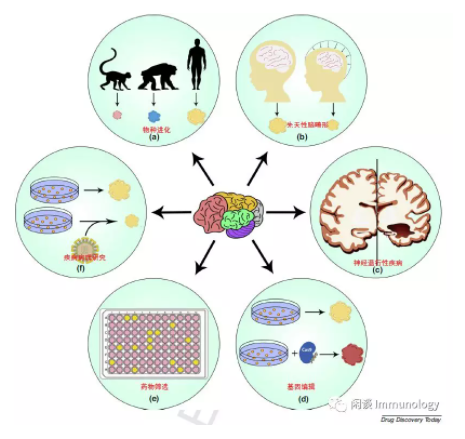
三)神经类器官的各种应用
物种进化
先天性脑畸形
神经退行性疾病
基因编辑
药物筛选
疾病病理学研究
参考资料:
[1]Yotam E. Bar-Ephraim, Kai Kretzschmarand Hans Clevers,Organoids in immunological research,Nature Reviews Immunology,2019
[2]Tanya Chhibber et al,CNS organoids: an innovative tool for neurological disease modeling and drug neurotoxicity screening,Drug Discovery Today, November 2019
[3]Richard J. Mills et al, Drug Screening in Human PSC-Cardiac Organoids Identifies Pro-proliferative Compounds Acting via the Mevalonate Pathway,Cell Stem Cell 24, 895–907, June 6, 2019
该文章来自于网络转载,版权归原作者所有。如有涉及侵权请给予告知,我们将尽快删除相关内容。